Cơ Chế Phản Ứng Hóa Học Của Ắc Quy Axit: Nguyên Lý Vận Hành Và Bằng Chứng Khoa Học Từ Ắc Quy Đồng Khánh
Phân tích các phản ứng hóa học chủ chốt của ắc quy axit, làm sáng tỏ cách chúng tích lũy và giải phóng năng lượng. Hãy đọc bài viết này từ Ắc Quy Đồng Khánh để cập nhật kiến thức khoa học chuẩn xác. I. Mở đầu Trong thời đại kỹ thuật số, ắc quy axit-chì đã trở thành một giải pháp cực kỳ quan trọng và phổ biến. Mặc dù phổ biến, hiểu biết về cơ chế bên trong của chúng, đặc biệt là những chuyển hóa hóa học cốt lõi giúp chúng tích trữ và giải phóng điện năng. Hiểu rõ các biến đổi hóa học trong ắc quy axit không chỉ mang lại kiến thức sâu sắc mà còn đóng vai trò then chốt trong quá trình bảo dưỡng và sử dụng hiệu quả cũng như thúc đẩy nghiên cứu công nghệ pin. Kiến thức này giúp chúng ta giải thích những vấn đề như giảm dung lượng, độ bền của ắc quy và phương pháp cải thiện hiệu suất. Nhằm cung cấp một cái nhìn toàn diện và sâu sắc về cách thức hoạt động của ắc quy axit, nội dung này sẽ làm rõ những phản ứng hóa học cốt lõi xảy ra trong chu trình nạp và phóng điện. Chúng tôi sẽ trình bày các phương trình hóa học minh họa rõ ràng, kèm theo dẫn chứng khoa học và minh họa cụ thể, nhằm giúp quý độc giả nắm bắt kiến thức một cách chính xác và dễ hiểu nhất. Phần thân bài Các bộ phận phản ứng cốt lõi của ắc quy axit Trước khi đi sâu vào các phản ứng hóa học, việc nhận diện các thành phần chủ yếu trong ắc quy axit-chì là điều cần thiết. Mỗi yếu tố đều có chức năng quan trọng trong việc lưu trữ và giải phóng điện năng. Điện cực âm (chì, Pb) và điện cực dương (chì dioxide, PbO2) Điện cực âm: Là vật liệu chì tinh khiết (Pb), thường ở dạng cấu trúc xốp nhằm tối đa hóa diện tích tiếp xúc với dung dịch điện phân. Trong quá trình xả, bản cực này đóng vai trò là nơi giải phóng electron. Điện cực dương: Là vật liệu chì dioxide (PbO2), cũng có cấu trúc xốp. Trong quá trình xả, bản cực này là nơi nhận electron. Môi trường phản ứng chính: dung dịch axit sulfuric 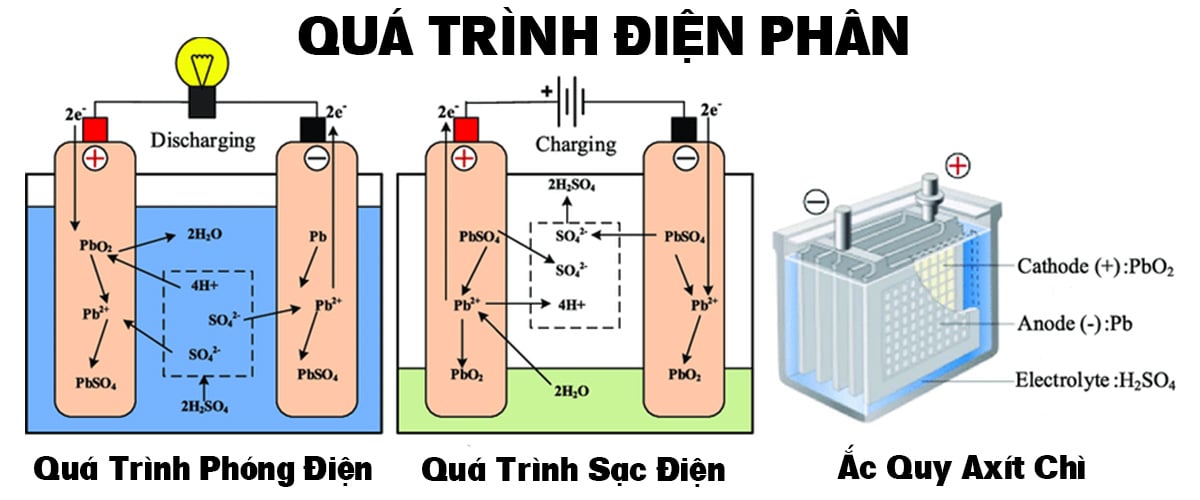 Dung dịch điện phân trong ắc quy axit-chì là axit sulfuric (H2SO4) được pha loãng. Axit sulfuric phân tách thành ion H+ và SO4^2-, có chức năng quan trọng trong việc di chuyển ion giữa hai điện cực và trực tiếp tham gia vào các phản ứng hóa học. Nồng độ axit sulfuric biến đổi trong suốt chu trình nạp và phóng điện, là một thước đo quan trọng để đánh giá trạng thái hoạt động của ắc quy. Sự hình thành chì sulfat (PbSO4) trong quá trình vận hành Chì sulfat (PbSO4) là hợp chất được tạo ra trên bề mặt cả hai điện cực trong quá trình phóng điện. Mặc dù cần thiết cho quá trình chuyển hóa năng lượng, nhưng sự tích tụ quá mức của PbSO4 có thể gây ra hiện tượng sulfat hóa, làm giảm hiệu suất và tuổi thọ của ắc quy. Cơ chế hóa học trong quá trình xả của ắc quy Khi ắc quy axit-chì cấp điện cho một thiết bị, nó đang ở trạng thái phóng điện. Trong giai đoạn này, năng lượng hóa học được biến đổi thành điện năng thông qua các phản ứng oxy hóa-khử xảy ra tại các điện cực. Phản ứng ở điện cực âm (chì, Pb): Pb(s) + SO4^2-(aq) → PbSO4(s) + 2e− Giải thích: Ở điện cực âm, chì (Pb) bị oxy hóa, kết hợp với ion sulfat (SO4^2-) trong dung dịch axit sulfuric để tạo ra chì sulfat (PbSO4) và giải phóng hai electron (2e−). Những electron này sẽ dịch chuyển qua mạch điện bên ngoài, tạo ra dòng điện. b. Phản ứng tại cực dương (chì oxit, PbO2): PbO2(s) + SO4^2-(aq) + 4H+(aq) + 2e− → PbSO4(s) + 2H2O(l) Diễn giải: Tại bản cực dương, chì oxit (PbO2) bị khử, phản ứng với ion sulfat (SO4^2-) và ion hydro (H+) từ axit sulfuric, đồng thời nhận hai electron (2e−) từ mạch ngoài để tạo thành chì sulfat (PbSO4) và nước (H2O). c. Tổng hợp phản ứng chung khi ắc quy xả: Bằng cách cộng hai phản ứng bán phần trên, chúng ta có thể thu được phương trình phản ứng tổng quát cho quá trình xả của ắc quy axit-chì: Pb(s) + PbO2(s) + 2H2SO4(aq) → 2PbSO4(s) + 2H2O(l) Trong quá trình xả, cả chì và chì oxit đều chuyển hóa thành chì sulfat, và axit sulfuric bị tiêu thụ, tạo ra nước. Đây là lý do tại sao nồng độ axit trong ắc quy giảm dần khi nó phóng điện. d. Nguyên lý hoạt động của acquy axit thích: Trong quá trình này, các muối sunfat chì (PbSO4) hình thành trên các bản cực, dẫn đến giảm hiệu suất. Chì sulfat (PbSO4) là một chất kết tủa màu trắng, có tính cách điện, bám dính vào bề mặt của cả hai điện cực. Khi ắc quy xả, lớp PbSO4 này ngày càng dày lên, làm giảm diện tích bề mặt hoạt động của các bản cực và cản trở sự tiếp xúc giữa chất điện phân với vật liệu hoạt động. Hiện tượng này, được gọi là sulfat hóa, làm giảm khả năng cung cấp dòng điện và dung lượng của ắc quy. Nếu ắc quy bị phóng điện quá mức và không được nạp lại nhanh chóng, các tinh thể PbSO4 có thể cứng lại và khó chuyển đổi trở lại, dẫn đến tình trạng chai ắc quy không thể phục hồi. Phản ứng hóa học trong quá trình sạc Để ắc quy có thể được sử dụng lại, việc nạp điện là cần thiết. Quá trình sạc là quá trình đảo ngược của quá trình xả, nơi năng lượng điện từ nguồn sạc được chuyển hóa trở lại thành năng lượng hóa học và tích trữ trong ắc quy. a. Dòng điện nguồn cung cấp ngược, phản ứng đảo chiều Khi dòng điện từ nguồn sạc được đưa vào ắc quy, các phản ứng hóa học diễn ra theo chiều ngược lại so với quá trình xả.
Dung dịch điện phân trong ắc quy axit-chì là axit sulfuric (H2SO4) được pha loãng. Axit sulfuric phân tách thành ion H+ và SO4^2-, có chức năng quan trọng trong việc di chuyển ion giữa hai điện cực và trực tiếp tham gia vào các phản ứng hóa học. Nồng độ axit sulfuric biến đổi trong suốt chu trình nạp và phóng điện, là một thước đo quan trọng để đánh giá trạng thái hoạt động của ắc quy. Sự hình thành chì sulfat (PbSO4) trong quá trình vận hành Chì sulfat (PbSO4) là hợp chất được tạo ra trên bề mặt cả hai điện cực trong quá trình phóng điện. Mặc dù cần thiết cho quá trình chuyển hóa năng lượng, nhưng sự tích tụ quá mức của PbSO4 có thể gây ra hiện tượng sulfat hóa, làm giảm hiệu suất và tuổi thọ của ắc quy. Cơ chế hóa học trong quá trình xả của ắc quy Khi ắc quy axit-chì cấp điện cho một thiết bị, nó đang ở trạng thái phóng điện. Trong giai đoạn này, năng lượng hóa học được biến đổi thành điện năng thông qua các phản ứng oxy hóa-khử xảy ra tại các điện cực. Phản ứng ở điện cực âm (chì, Pb): Pb(s) + SO4^2-(aq) → PbSO4(s) + 2e− Giải thích: Ở điện cực âm, chì (Pb) bị oxy hóa, kết hợp với ion sulfat (SO4^2-) trong dung dịch axit sulfuric để tạo ra chì sulfat (PbSO4) và giải phóng hai electron (2e−). Những electron này sẽ dịch chuyển qua mạch điện bên ngoài, tạo ra dòng điện. b. Phản ứng tại cực dương (chì oxit, PbO2): PbO2(s) + SO4^2-(aq) + 4H+(aq) + 2e− → PbSO4(s) + 2H2O(l) Diễn giải: Tại bản cực dương, chì oxit (PbO2) bị khử, phản ứng với ion sulfat (SO4^2-) và ion hydro (H+) từ axit sulfuric, đồng thời nhận hai electron (2e−) từ mạch ngoài để tạo thành chì sulfat (PbSO4) và nước (H2O). c. Tổng hợp phản ứng chung khi ắc quy xả: Bằng cách cộng hai phản ứng bán phần trên, chúng ta có thể thu được phương trình phản ứng tổng quát cho quá trình xả của ắc quy axit-chì: Pb(s) + PbO2(s) + 2H2SO4(aq) → 2PbSO4(s) + 2H2O(l) Trong quá trình xả, cả chì và chì oxit đều chuyển hóa thành chì sulfat, và axit sulfuric bị tiêu thụ, tạo ra nước. Đây là lý do tại sao nồng độ axit trong ắc quy giảm dần khi nó phóng điện. d. Nguyên lý hoạt động của acquy axit thích: Trong quá trình này, các muối sunfat chì (PbSO4) hình thành trên các bản cực, dẫn đến giảm hiệu suất. Chì sulfat (PbSO4) là một chất kết tủa màu trắng, có tính cách điện, bám dính vào bề mặt của cả hai điện cực. Khi ắc quy xả, lớp PbSO4 này ngày càng dày lên, làm giảm diện tích bề mặt hoạt động của các bản cực và cản trở sự tiếp xúc giữa chất điện phân với vật liệu hoạt động. Hiện tượng này, được gọi là sulfat hóa, làm giảm khả năng cung cấp dòng điện và dung lượng của ắc quy. Nếu ắc quy bị phóng điện quá mức và không được nạp lại nhanh chóng, các tinh thể PbSO4 có thể cứng lại và khó chuyển đổi trở lại, dẫn đến tình trạng chai ắc quy không thể phục hồi. Phản ứng hóa học trong quá trình sạc Để ắc quy có thể được sử dụng lại, việc nạp điện là cần thiết. Quá trình sạc là quá trình đảo ngược của quá trình xả, nơi năng lượng điện từ nguồn sạc được chuyển hóa trở lại thành năng lượng hóa học và tích trữ trong ắc quy. a. Dòng điện nguồn cung cấp ngược, phản ứng đảo chiều Khi dòng điện từ nguồn sạc được đưa vào ắc quy, các phản ứng hóa học diễn ra theo chiều ngược lại so với quá trình xả.  Tại cực âm (bản chì sulfat, PbSO4): PbSO4(s) + 2e− → Pb(s) + SO4^2-(aq) Chì sulfat (PbSO4) trên điện cực âm hấp thụ electron và biến đổi trở lại thành chì (Pb) cùng với việc giải phóng ion sulfat (SO4^2-). Ở điện cực dương (chì sulfat, PbSO4): PbSO4(s) + 2H2O(l) → PbO2(s) + SO4^2-(aq) + 4H+(aq) + 2e− Chì sulfat (PbSO4) trên điện cực dương tương tác với nước (H2O), giải phóng ion sulfat (SO4^2-) và ion hydro (H+), đồng thời biến đổi trở lại thành chì dioxide (PbO2) và giải phóng electron. Chì sulfat hòa tan, điện cực phục hồi trạng thái ban đầu (Pb và PbO2) Phản ứng tổng quát khi ắc quy nạp điện: 2PbSO4(s) + 2H2O(l) → Pb(s) + PbO2(s) + 2H2SO4(aq)
Tại cực âm (bản chì sulfat, PbSO4): PbSO4(s) + 2e− → Pb(s) + SO4^2-(aq) Chì sulfat (PbSO4) trên điện cực âm hấp thụ electron và biến đổi trở lại thành chì (Pb) cùng với việc giải phóng ion sulfat (SO4^2-). Ở điện cực dương (chì sulfat, PbSO4): PbSO4(s) + 2H2O(l) → PbO2(s) + SO4^2-(aq) + 4H+(aq) + 2e− Chì sulfat (PbSO4) trên điện cực dương tương tác với nước (H2O), giải phóng ion sulfat (SO4^2-) và ion hydro (H+), đồng thời biến đổi trở lại thành chì dioxide (PbO2) và giải phóng electron. Chì sulfat hòa tan, điện cực phục hồi trạng thái ban đầu (Pb và PbO2) Phản ứng tổng quát khi ắc quy nạp điện: 2PbSO4(s) + 2H2O(l) → Pb(s) + PbO2(s) + 2H2SO4(aq)  Trong quá trình sạc, chì sulfat trên cả hai bản cực được chuyển hóa trở lại thành chì và chì oxit, đồng thời nước bị tiêu thụ và axit sulfuric được tái tạo. Điều này dẫn đến sự gia tăng nồng độ axit trong ắc quy, từ đó phục hồi khả năng lưu trữ năng lượng của nó. c. Quá trình này giúp pin có thể tái sử dụng nhiều lần, nhưng tuổi thọ giảm dần do tích tụ muối và hao mòn vật lý Mặc dù các phản ứng hóa học trong ắc quy axit-chì là thuận nghịch, cho phép ắc quy được sạc và xả nhiều lần, nhưng quá trình này không diễn ra hoàn hảo. Mỗi chu trình nạp/phóng điện đều dẫn đến một mức độ suy giảm nhất định. Một phần nhỏ chì sulfat có thể không hoàn nguyên hoàn toàn, dẫn đến sự tích tụ dần dần trên các bản cực. Bên cạnh đó, sự ăn mòn vật lý của các điện cực và việc nước bay hơi (đối với ắc quy nước) cũng góp phần làm giảm tuổi thọ của ắc quy theo thời gian. Đây là lý do tại sao ắc quy có tuổi thọ giới hạn và cần được thay thế sau một thời gian sử dụng nhất định. Nghiên cứu khoa học và thực tiễn Các phản ứng hóa học trong ắc quy axit-chì không chỉ dừng lại ở lý thuyết mà đã được xác nhận và áp dụng phổ biến trong suốt quá trình phát triển của công nghệ pin. Nghiên cứu khoa học đã khẳng định phản ứng chì – sulfat là cơ sở của công nghệ pin axit-chì Kể từ khi Gaston Planté phát minh ra ắc quy axit-chì vào năm 1859, hàng loạt các nghiên cứu khoa học chuyên sâu về điện hóa học đã được thực hiện để làm rõ cơ chế hoạt động của nó. Các nhà khoa học đã sử dụng nhiều kỹ thuật phân tích tiên tiến để quan sát trực tiếp sự hình thành và phân hủy của chì sulfat trên các bản cực, cũng như sự thay đổi nồng độ axit sulfuric. Những nghiên cứu này đã cung cấp bằng chứng vững chắc cho thấy phản ứng chì-sulfat chính là nền tảng cơ bản, quyết định khả năng lưu trữ và giải phóng năng lượng của ắc quy axit-chì. Cái nhìn sâu sắc này đã tạo điều kiện cho việc cải tiến vật liệu và thiết kế ắc quy. b. Thông tin từ các nhà sản xuất, trong đó có Ắc Quy Đồng Khánh, về phản ứng hóa học giúp tối ưu hóa quá trình hoạt động của ắc quy Các nhà sản xuất ắc quy hàng đầu thế giới, trong đó có Ắc Quy Đồng Khánh, luôn dựa vào kiến thức sâu rộng về các phản ứng hóa học này để thiết kế và sản xuất ắc quy. Họ sử dụng các công nghệ tiên tiến để kiểm soát kích thước tinh thể PbSO4, tối ưu hóa cấu trúc xốp của bản cực, và đảm bảo chất lượng dung dịch điện phân. Chẳng hạn, việc bổ sung các chất phụ gia đặc biệt vào vật liệu điện cực có thể giúp giảm thiểu hiện tượng sulfat hóa và gia tăng tuổi thọ chu kỳ của ắc quy. Thông tin kỹ thuật từ các nhà sản xuất thường xuyên nhấn mạnh tầm quan trọng của việc duy trì các điều kiện hoạt động lý tưởng để các phản ứng hóa học diễn ra hiệu quả nhất. c. Ảnh hưởng của phản ứng lên tuổi thọ và hiệu suất của ắc quy trong sử dụng thực tế Trong sử dụng thực tế, các yếu tố như nhiệt độ môi trường, thói quen sạc/xả, và tần suất sử dụng đều ảnh hưởng trực tiếp đến tốc độ và hiệu quả của các phản ứng hóa học bên trong ắc quy. Chẳng hạn, nhiệt độ cao làm tăng tốc độ các phản ứng phụ và thúc đẩy quá trình sulfat hóa, trong khi việc phóng điện sâu liên tục có thể dẫn đến sự hình thành các tinh thể PbSO4 cứng khó phục hồi. Nắm vững những tác động này giúp người dùng áp dụng các biện pháp bảo dưỡng thích hợp, như tránh để ắc quy cạn kiệt hoàn toàn, nạp điện định kỳ, và bảo vệ ắc quy khỏi nhiệt độ quá cao hoặc quá thấp, từ đó tối ưu hóa tuổi thọ và hiệu suất của ắc quy. Tổng kết Tóm lại, cơ chế hoạt động của ắc quy axit-chì là bằng chứng rõ ràng cho sự chuyển hóa năng lượng hóa học thành điện năng và ngược lại, thông qua hàng loạt các phản ứng oxy hóa-khử có thể đảo ngược. Các phản ứng cốt lõi xảy ra tại điện cực âm (chì) và điện cực dương (chì dioxide) với sự tham gia của axit sulfuric, tạo thành chì sulfat khi phóng điện và phục hồi các vật liệu ban đầu khi nạp điện. Nắm vững các phản ứng hóa học này là yếu tố then chốt để tối ưu hóa hoạt động và kéo dài tuổi thọ của ắc quy. Để đảm bảo ắc quy của bạn luôn vận hành hiệu quả và bền bỉ, hãy thực hiện bảo trì đúng phương pháp và chọn lựa sản phẩm có chất lượng cao. Nếu quý vị cần hướng dẫn chi tiết hoặc mua sắm các loại ắc quy chính hãng với công nghệ mới nhất dựa trên các nguyên tắc khoa học đã được kiểm chứng, hãy tìm đến Ắc Quy Đồng Khánh ngay hôm nay. Chúng tôi luôn sẵn sàng đồng hành cùng bạn để đảm bảo nguồn năng lượng ổn định cho mọi nhu cầu.
Trong quá trình sạc, chì sulfat trên cả hai bản cực được chuyển hóa trở lại thành chì và chì oxit, đồng thời nước bị tiêu thụ và axit sulfuric được tái tạo. Điều này dẫn đến sự gia tăng nồng độ axit trong ắc quy, từ đó phục hồi khả năng lưu trữ năng lượng của nó. c. Quá trình này giúp pin có thể tái sử dụng nhiều lần, nhưng tuổi thọ giảm dần do tích tụ muối và hao mòn vật lý Mặc dù các phản ứng hóa học trong ắc quy axit-chì là thuận nghịch, cho phép ắc quy được sạc và xả nhiều lần, nhưng quá trình này không diễn ra hoàn hảo. Mỗi chu trình nạp/phóng điện đều dẫn đến một mức độ suy giảm nhất định. Một phần nhỏ chì sulfat có thể không hoàn nguyên hoàn toàn, dẫn đến sự tích tụ dần dần trên các bản cực. Bên cạnh đó, sự ăn mòn vật lý của các điện cực và việc nước bay hơi (đối với ắc quy nước) cũng góp phần làm giảm tuổi thọ của ắc quy theo thời gian. Đây là lý do tại sao ắc quy có tuổi thọ giới hạn và cần được thay thế sau một thời gian sử dụng nhất định. Nghiên cứu khoa học và thực tiễn Các phản ứng hóa học trong ắc quy axit-chì không chỉ dừng lại ở lý thuyết mà đã được xác nhận và áp dụng phổ biến trong suốt quá trình phát triển của công nghệ pin. Nghiên cứu khoa học đã khẳng định phản ứng chì – sulfat là cơ sở của công nghệ pin axit-chì Kể từ khi Gaston Planté phát minh ra ắc quy axit-chì vào năm 1859, hàng loạt các nghiên cứu khoa học chuyên sâu về điện hóa học đã được thực hiện để làm rõ cơ chế hoạt động của nó. Các nhà khoa học đã sử dụng nhiều kỹ thuật phân tích tiên tiến để quan sát trực tiếp sự hình thành và phân hủy của chì sulfat trên các bản cực, cũng như sự thay đổi nồng độ axit sulfuric. Những nghiên cứu này đã cung cấp bằng chứng vững chắc cho thấy phản ứng chì-sulfat chính là nền tảng cơ bản, quyết định khả năng lưu trữ và giải phóng năng lượng của ắc quy axit-chì. Cái nhìn sâu sắc này đã tạo điều kiện cho việc cải tiến vật liệu và thiết kế ắc quy. b. Thông tin từ các nhà sản xuất, trong đó có Ắc Quy Đồng Khánh, về phản ứng hóa học giúp tối ưu hóa quá trình hoạt động của ắc quy Các nhà sản xuất ắc quy hàng đầu thế giới, trong đó có Ắc Quy Đồng Khánh, luôn dựa vào kiến thức sâu rộng về các phản ứng hóa học này để thiết kế và sản xuất ắc quy. Họ sử dụng các công nghệ tiên tiến để kiểm soát kích thước tinh thể PbSO4, tối ưu hóa cấu trúc xốp của bản cực, và đảm bảo chất lượng dung dịch điện phân. Chẳng hạn, việc bổ sung các chất phụ gia đặc biệt vào vật liệu điện cực có thể giúp giảm thiểu hiện tượng sulfat hóa và gia tăng tuổi thọ chu kỳ của ắc quy. Thông tin kỹ thuật từ các nhà sản xuất thường xuyên nhấn mạnh tầm quan trọng của việc duy trì các điều kiện hoạt động lý tưởng để các phản ứng hóa học diễn ra hiệu quả nhất. c. Ảnh hưởng của phản ứng lên tuổi thọ và hiệu suất của ắc quy trong sử dụng thực tế Trong sử dụng thực tế, các yếu tố như nhiệt độ môi trường, thói quen sạc/xả, và tần suất sử dụng đều ảnh hưởng trực tiếp đến tốc độ và hiệu quả của các phản ứng hóa học bên trong ắc quy. Chẳng hạn, nhiệt độ cao làm tăng tốc độ các phản ứng phụ và thúc đẩy quá trình sulfat hóa, trong khi việc phóng điện sâu liên tục có thể dẫn đến sự hình thành các tinh thể PbSO4 cứng khó phục hồi. Nắm vững những tác động này giúp người dùng áp dụng các biện pháp bảo dưỡng thích hợp, như tránh để ắc quy cạn kiệt hoàn toàn, nạp điện định kỳ, và bảo vệ ắc quy khỏi nhiệt độ quá cao hoặc quá thấp, từ đó tối ưu hóa tuổi thọ và hiệu suất của ắc quy. Tổng kết Tóm lại, cơ chế hoạt động của ắc quy axit-chì là bằng chứng rõ ràng cho sự chuyển hóa năng lượng hóa học thành điện năng và ngược lại, thông qua hàng loạt các phản ứng oxy hóa-khử có thể đảo ngược. Các phản ứng cốt lõi xảy ra tại điện cực âm (chì) và điện cực dương (chì dioxide) với sự tham gia của axit sulfuric, tạo thành chì sulfat khi phóng điện và phục hồi các vật liệu ban đầu khi nạp điện. Nắm vững các phản ứng hóa học này là yếu tố then chốt để tối ưu hóa hoạt động và kéo dài tuổi thọ của ắc quy. Để đảm bảo ắc quy của bạn luôn vận hành hiệu quả và bền bỉ, hãy thực hiện bảo trì đúng phương pháp và chọn lựa sản phẩm có chất lượng cao. Nếu quý vị cần hướng dẫn chi tiết hoặc mua sắm các loại ắc quy chính hãng với công nghệ mới nhất dựa trên các nguyên tắc khoa học đã được kiểm chứng, hãy tìm đến Ắc Quy Đồng Khánh ngay hôm nay. Chúng tôi luôn sẵn sàng đồng hành cùng bạn để đảm bảo nguồn năng lượng ổn định cho mọi nhu cầu.